Unsere Labore
In unserer Analytik kommen moderne Chromatographie Systeme von Waters und Agilent zum Einsatz. Hierbei sind alle Waters H-Class UPLC Systeme, neben einem klassischen UV/VIS (PDA) Detektoren, zusätzlich mit eine, QDa-Detektoren (single MS) zur massenspektrometrischen Bestimmung ausgestattet. Die Agilent 1260 HPLC-Systemen inklusive DAD (UV/VIS)-Detektoren komplettieren unser Equipment und sind insbesondere für Routinemethoden im QC-Bereich sehr gut geeignet. Präzise Stabilitätskammern erlauben uns verlässliche Stabilitätsprognosen basieren auf akzelerierten Stabilitätsstudien.
Neben einem modernen Equipment erfordert die Probenaufarbeitung insbesondere von halbfesten Formulierungen weiterhin viel Wissen, Erfahrung und Geschick.
Zur Entwicklung und Labormaßstabs-Herstellung von flüssigen und halbfesten Formulierungen nutzen wir verschiedene Homogenisatoren und Rührer. Unsere wichtigsten Technologien zur physikalischen Formulierungscharakterisierung sind Mikroskopie und Rheologie, die wir an einem Anton Paar MCR102 Hochleistungs-Rheometer durchführen. Eine Sicherheitswägekabine erlaubt uns die Handhabung hochaktiver Substanzen.
Für in vitro Release (IVRT) und in vitro Permeationstest (IVPT) nutzen wir die fortschrittliche Technologie Teledyne Hanson Robotic Diffusion Station (RDS).
Warum RaDes
Wir schaffen aus Konzepten und Wirkstoffen technisch robuste, regulatorisch überzeugende und patientenfreundliche Produkte, deren Exklusivität bestmöglich geschützt ist.
Zusammen mit unseren Kunden erarbeiten wir individuelle, der jeweiligen Problemstellung angepasste Lösungen, um den besten Wert für die eingesetzten Ressourcen erreichen.
Wir verfolgen den Ansatz des „rationalen Designs“, um Formulierungen und analytische Methoden zielgerichtet und robust zu entwickeln und damit Lösungen bereitzustellen, die Risiken und Kosten reduzieren.
Halbfeste Formulierungen sind oft komplex und in ihren kritischen Qualitätsattributen allgemein weniger gut verstanden als z.B. typische feste Arzneiformen. Deshalb werden diese meist noch empirisch, d.h. durch Ausprobieren bekannter Ansätze, entwickelt, bis ein Weg gefunden ist, der zu akzeptablen Ergebnissen führt. Im Gegensatz zu diesem Ansatz von „Qualität durch Ausprobieren“, verfolgen wir ein rationales Design basierend auf einem systematischen Verständnis der Formulierungen hinsichtlich chemischer und physikalischer Stabilität, (Haut)-Penetrationsvermögen und kosmetischer Eigenschaften, welches „Quality by Design“ liefert. Diese Herangehensweise führt erfahrungsgemäß schneller zu einem robusten, marktfähigen Produkt, kann bei Bedarf zielgerichtet modifiziert werden und erlaubt eine gezielte Risiko-Minimierung, sowohl in technischer, regulatorischer und ökonomischer Sicht.
Cremes sind traditionelle Arzneiformen, deren Potential aber noch nicht ausgeschöpft ist. Wir haben durch systematische Studien tiefere Einsichten in Emulsionssysteme gewonnen, die es uns erlauben, eine Vielzahl von Formulierungsproblemen zu lösen.
Wir bieten Lösungen für Formulierungsherausforderungen wie Solubilisierung, chemische Stabilisierung und Steuerung der Freisetzung und Hautpenetration von Wirkstoffen in Cremes, genauer: viskositätsstabilisierten Emulsionssystemen, an. Für die genannten Herausforderungen gab es in den vergangenen Jahrzehnten viele Versuche, diese mit „Special/Novel Delivery Systems“ zu lösen, die aber nur zu sehr wenigen Marktprodukten führten. Solche partikel-basierten Systeme sind außerdem typischerweise regulatorisch aufwändig, schwerer in robuste Routine-Prozesse zu überführen und mit höheren Investitions- und Herstellungskosten verbunden.
Basierend auf einem grundlegenden Verständnis von Emulsionen hinsichtlich ihrer thermodynamischen Grundlagen, können wir – als „Creme 2.0“ – für viele dieser Herausforderungen gezielt entwickelte Cremes anbieten, die wesentlich schneller, kostengünstiger und risikoärmer zur Marktreife zu bringen sind.
Eine Grundlagenstudie von Mitarbeitern der RaDes GmbH in Zusammenarbeit mit der TU Braunschweig zur systematischen Optimierung von Konservierungsmittelsystemen in Cremes wurde kürzlich publiziert (https://www.sciencedirect.com/science/article/abs/pii/S0939641118308026). Die Publikation einer Arbeit zur gezielten Stabilisierung hydrolyseempfindlicher Wirkstoffe in Cremes ist in Vorbereitung.
Dabei sind wir nicht auf Cremes fixiert, sondern fokussieren uns darauf, jeweils die bestmögliche Lösung für die spezifische Formulierungsherausforderung zu identifizieren. Auch für Hydro- oder Oleogele, Salben, (filmbildende) Lösungen und weitere Formate verfügen wir über reiche Erfahrung.
Die Prototypenentwicklung ist nur der Beginn des Lebenszyklus einer Formulierung. Wir berücksichtigen von Anfang an die Einflüsse auf das zukünftige Potential sowie Risiken und Kosten.
Bezogen auf die Gesamtentwicklungskosten eines Medikaments ist die explorative Entwicklung einer Formulierung in der Regel günstig. Allerdings wird mit der Auswahl eines finalen Prototyps eine strategisch und ökonomisch folgenreiche Entscheidung getroffen. Die Summe aus zukünftigen Ausgaben hinsichtlich Investitions-, Betriebs- und Herstellkosten sowie der Aufwand für Freigabeuntersuchungen und regulatorische Betreuung können sich für verschiedene Prototypen um mehrere Millionen Euro unterscheiden. Wir sind in der Lage, solche in die Zukunft projizierten Eigenschaften von Prototypen zu bewerten und basierend auf Risikoanalysen Szenarien zu erstellen, die es unseren Kunden erlauben, zusammen mit uns nachhaltig optimierte Lösungen zu entwickeln.
In flüssigen und halbfesten Formulierungen sind Wirkstoffe häufig gelöst und können vielfältig reagieren, was oft eine zusätzliche Stabilisierung erfordert. Ebenso stellen das ungünstige Wirkstoff zu Matrix-Verhältnis und die quantitative Extraktion aus der Grundlage häufig Herausforderungen dar, für die wir Lösungen bereithalten.
Wir verfügen über eine führende Expertise zur analytischen Methodenentwicklung und -validierung, insbesondere auch für schwierig zu analysierende halbfeste Produkte (z.B. bei problematischer Extraktion, niedriger Dosis, geringer UV-Aktivität, sowie zur Strukturaufklärung bei komplexen Abbauwegen). Dies verbinden wir mit einer umfangreichen Erfahrung in Bezug auf chemische Stabilisierung (Verminderung von Oxidation, Hydrolyse oder Isomerisierung) und zur Interaktion von Wirk- und Hilfsstoffen mit Packmitteln. Ebenso sind wir in der Lage, Risikobewertungen von sekundären Abbauphänomenen, wie z.B. Reaktionen von bzw. mit Abbauprodukten von Wirk- und Hilfsstoffen zu erstellen. Diese folgen oft einer nicht-linearen, komplexen Kinetik und sind aus der routinemäßigen Betrachtung von Kurzzeitstabilitätsdaten nicht vorhersagbar.
Performance Testing
RaDes hat eine Reihe moderner in vitro und ex vivo Modelle zur systematischen Risikominimierung dermaler Entwicklungsprojekte und für Performance- und Qualitätsuntersuchungen topischer Formulierungen entwickelt. Diese Modelle bieten Unterstützung über den gesamten Lebenszyklus der Arzneimittel von der Auswahl des Wirkstoffkandidaten und der Formulierung bis hin zu Bioäquivalenztests und Änderungen bei zugelassenen Produkten. Für eine sensitive und selektive Analytik dieser Studien verfügen wir über leistungsstarkes analytisches Equipment.
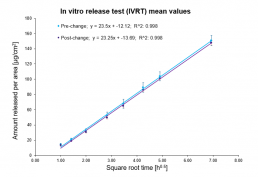
- Bestimmung der Freisetzungsrate durch Filtermembranen
- Ranking und Auswahl von Formulierungsprototypen für dermale und transdermale Applikation
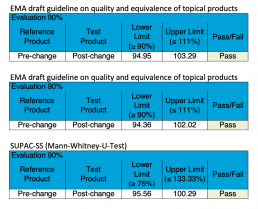
- Evaluierung der Äquivalenz topischer Produkte für generische Zulassungsverfahren gemäß „EMA Draft guideline on quality and equivalence of topical products”
- Änderungen an zugelassenen Arzneimitteln („Scale-up and post approval changes“ gemäß SUPACC SS)
- Unterstützung von initialen Assessments bis zu voll validierten Methoden gemäß OECD, FDA oder EMA Richtlinien, einschließlich der analytischen Methodenvalidierung gemäß ICH Richtlinien.
- Studien mittels “Robotic diffusion system” (RDS) mit Trockenheizblocks und optimierter Rührergeometrie für verbesserte Datenqualität. Parallele Durchführung mit 12 vertikalen Diffusionszellen.
- Eine Einführung von RaDes zu IVRT mit Beispielen ist als Webinar-Aufzeichnung hier (YouTube) verfügbar.
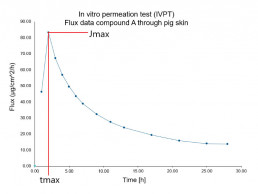
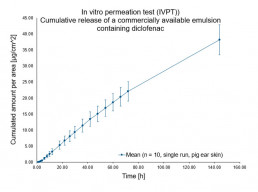
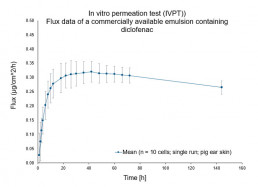
- Evaluierung des charakteristischen Permeationsprofils eines Wirk- /Inhaltsstoffs (“flux rate”, “amount permeated”) durch menschliche oder tierische Haut)
- Auswahl von Wirkstoffkandidaten und Formulierungsprototypen zur Risikominimierung des klinischen Programms.
- Bioäquivalenzstudien für topische Generika gemäß der “EMA Draft guideline on quality and equivalence of topical products”
- Absorptionsuntersuchungen für die Sicherheitsbewertung von Chemikalien, Pestiziden, etc. gemäß OECD 428
- In vitro dermal Absorptionsstudien für Kosmetika gemäß der “Scientific Committee on Consumer Safety” (SCCS) Richtlinie
- Änderungen an zugelassenen Arzneimitteln („Scale-up and post approval changes“ gemäß SUPACC SS)
- Unterstützung von initialen Assessments bis zu voll validierten Methoden gemäß OECD, FDA oder EMA Richtlinien, einschließlich der analytischen Methodenvalidierung gemäß ICH Richtlinien.
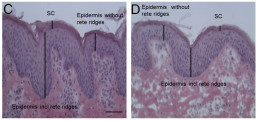
- Untersuchung der Verteilung von Wirkstoffen zwischen Epidermis und Dermis (heat splitting)
- Eigene Präparierung der Schweinehaut. Verwendung von frischer Haut auf Nachfrage möglich
- Optional Nutzung von künstlichen Strat-M® Membranen (nicht-tierischer Ursprung) zum Screening des Permeationspotentials topischer Formulierungen und transdermaler Pflaster
- Studien mittels “Robotic diffusion system” (RDS) mit Trockenheizblocks und optimierten Rührergeometrien für verbesserte Datenqualität. Parallele Durchführung mit 12 vertikalen Diffussionszellen
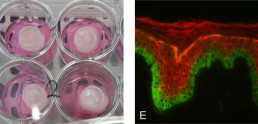
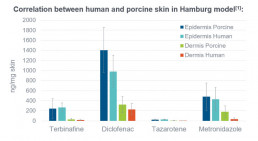
- Innovatives Hautpenetrationsmodell unter Verwendung viabler Schweinehaut. Exzellente Korrelation mit viabler Humanhaut nachgewiesen.
- Ermöglicht die Bestimmung genauer Biodistributionsmuster von applizierten Wirkstoffen in der Haut
- Liefert Penetrationsprofile in verschiedenen Hautschichten. Eine direkte Bestimmung der Wirkstoffkonzentration am Wirkort in der Haut ist möglich
- Kosteneffizient und ohne ethische Vorbehalte
- Durchführung in Zusammenarbeit mit dem Universitätsklinikum Hamburg Eppendorf (UKE). Analytische Methodenentwicklung und Probenaufbereitung und Bioanalytik bei RaDes
- Viables Hautmodel, das die Bestimmung von Hautmetaboliten der Wirkstoffe erlaubt
- Siehe: Herbig ME, Houdek P, Gorissen S, Brandner J et al. A custom-tailored model to investigate skin penetration in porcine skin and its correlation with human skin. Eur J Pharm Biopharm, (95) 99-109, 2015
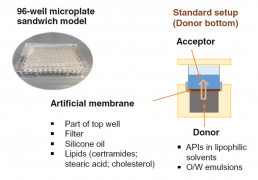
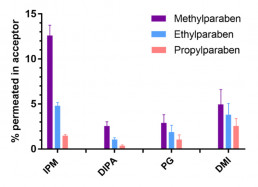
- Screening Tool für das Hautpermeationspotenzial von Wirkstoffen/Formulierungen
- 96-well plate-Format mit einer porösen, Lipid-imprägnierten Filtermembran, die das Stratum Corneum als Hauptpenetrations-Barriere für dermale Absorption nachbildet
- Erlaubt Ranking und Auswahl von topischen und transdermalen Formulierungen
- RaDes Untersuchungen haben zum Verständnis der Möglichkeiten und Limitationen des Modells beigetragen. Siehe: Köllmer M et al. Investigation of the Compatibility of the Skin PAMPA Model with Topical Formulation and Acceptor Media Additives Using Different Assay Setups. AAPS PharmSciTech, 20(89), 2019.
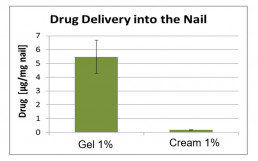
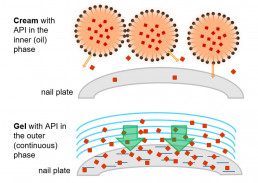
Der Nagel stellt eine fundamental unterschiedliche Barriere als die Haut dar und erfordert deshalb grundlegend unterschiedliche Formulierungskonzepte und Penetrationsmodelle.
- Intern entwickeltes Modell unter Verwendung menschlicher „Nail Clippings“ zur Bestimmung der in die Nagelplatte eingedrungenen Wirkstoffkonzentration
- Da die Quellung des Nagels die Penetration von Stoffen erleichtert, bieten wir auch ein Modell zur Charakterisierung des Nagelquell-Potentials von Formulierungen
Sascha Gorissen
+49 151 12986843
sascha.gorissen@rades-development.com

Dr. Petra Lohmann
Seit Januar 2020 leitet Frau Dr. Lohmann die Qualitätssicherung der RaDes GmbH. Sie hat an der Universität Münster sowohl Chemie als auch Pharmazie studiert und in Pharmazeutischer Chemie promoviert. Nach Tätigkeiten in der Analytik und Qualitätskontrolle bei Wyeth Pharma GmbH und Haupt Pharma GmbH, kam sie 2000 zur Hermal GmbH, wo sie für den Bereich R&D die Leitung der Qualitätskontrolle und ab 2005 die Funktion der Sachkundigen Person, sowie von 2013 bis 2016 die Leitung der Qualitätssicherung innehatte. Von 2016 bis 2019 leitete sie die Qualitätssicherung der Bode Chemie GmbH (Hartmann Gruppe), wo sie ein Portfolio von Medizinprodukten, Arzneimitteln, Bioziden und Kosmetika betreute.
Durch diese Tätigkeiten ist sie umfassend vertraut mit den Industrie-relevanten Qualitätsstandards und Regelwerken wie GMP, GCP, GLP, lSO 9001, ISO 13485, ISO 14001, AMG, AMWHV, 21 CFR 210/211, MPG und den Anforderungen der Arzneibücher, sowie mit der Bewertung und Genehmigung von Qualifizierungen und Validierungen, des Qualitätsmoduls von IMPDs und Zulassungsdossiers und der Zertifizierung klinischer Prüfpräparate. Weiterhin verfügt sie über reiche Erfahrung in der Planung und Durchführung interner und externer Audits und der Gestaltung von Verantwortungsabgrenzungen in Transfer- und Kollaborationsprojekten.
Frau Dr. Lohmann ist bei RaDes für den Aufbau und die Pflege eines Qualitätsmanagementsystems, sowie die Qualitätsstandards für Studien unter GxP, verantwortlich. Sie unterstützt die Kundenprojekte mit Strategien und Expertise in Qualitäts- und Compliance-Aspekten. Weiterhin bietet sie Beratung und Expertisen im Qualitätsmanagementbereich an, wie z.B. GMP-Schulungen, Unterstützung bei Behördeninspektionen und Beratung beim Aufbau und der Optimierung von Qualitätsmanagementsystemen.
Datenschutzerklärung
Mit dieser Datenschutzerklärung möchten wir Sie über die Erhebung personenbezogener Daten bei Nutzung unserer Website informieren.
1. Personenbezogene Daten
Personenbezogene Daten im Sinne des Art. 4 EU-Datenschutz-Grundverordnung (DSGVO) sind alle Informationen, die sich auf eine identifizierte oder identifizierbare natürliche Person beziehen, z. B. Name, Adresse und E-Mail-Adresse.
2. Verantwortlicher
Verantwortlicher für die Verarbeitung personenbezogener Daten im Sinne des Art. 4 (7) DSGVO ist RaDes GmbH, Schnackenburgallee 114, 22525, Hamburg (info@rades-development.com).
3. Erhebung und Verarbeitung personenbezogener Daten bei Besuch unserer Website
Beim Besuch unserer Website erheben wir nur die personenbezogenen Daten, die Ihr Browser an unseren Server übermittelt und die für die Darstellung unserer Website und die Gewährleistung von Stabilität und Sicherheit technisch notwendig sind.
Rechtsgrundlage ist Art. 6 1 b) DSGVO.
Cookies
Die Internetseiten verwenden teilweise so genannte Cookies. Cookies richten auf Ihrem Rechner keinen Schaden an und enthalten keine Viren. Cookies dienen dazu, unser Angebot nutzerfreundlicher, effektiver und sicherer zu machen. Cookies sind kleine Textdateien, die auf Ihrem Rechner abgelegt werden und die Ihr Browser speichert.
Die meisten der von uns verwendeten Cookies sind so genannte “Session-Cookies”. Sie werden nach Ende Ihres Besuchs automatisch gelöscht. Andere Cookies bleiben auf Ihrem Endgerät gespeichert bis Sie diese löschen. Diese Cookies ermöglichen es uns, Ihren Browser beim nächsten Besuch wiederzuerkennen.
Sie können Ihren Browser so einstellen, dass Sie über das Setzen von Cookies informiert werden und Cookies nur im Einzelfall erlauben, die Annahme von Cookies für bestimmte Fälle oder generell ausschließen sowie das automatische Löschen der Cookies beim Schließen des Browser aktivieren. Bei der Deaktivierung von Cookies kann die Funktionalität dieser Website eingeschränkt sein.
Cookies, die zur Durchführung des elektronischen Kommunikationsvorgangs oder zur Bereitstellung bestimmter, von Ihnen erwünschter Funktionen (z.B. Warenkorbfunktion) erforderlich sind, werden auf Grundlage von Art. 6 Abs. 1 lit. f DSGVO gespeichert. Der Websitebetreiber hat ein berechtigtes Interesse an der Speicherung von Cookies zur technisch fehlerfreien und optimierten Bereitstellung seiner Dienste. Soweit andere Cookies (z.B. Cookies zur Analyse Ihres Surfverhaltens) gespeichert werden, werden diese in dieser Datenschutzerklärung gesondert behandelt.
Server-Log-Dateien
Der Provider der Seiten erhebt und speichert automatisch Informationen in so genannten Server-Log-Dateien, die Ihr Browser automatisch an uns übermittelt. Dies sind:
- Browsertyp und Browserversion
- verwendetes Betriebssystem
- Referrer URL
- Hostname des zugreifenden Rechners
- Uhrzeit der Serveranfrage
- IP-Adresse
Eine Zusammenführung dieser Daten mit anderen Datenquellen wird nicht vorgenommen.
4. Kontaktaufnahme
Bei Kontaktaufnahme mit uns per E-Mail werden die von Ihnen mitgeteilten Daten (Ihre E-Mail-Adresse, ggf. Ihr Name und Ihre Telefonnummer bzw. andere angegebenen personenbezogenen Daten) von uns gespeichert, um Ihre Fragen zu beantworten oder um der für unsere Geschäftszwecke erforderlichen Kommunikation nachzukommen. Die in diesem Zusammenhang anfallenden Daten löschen wir wieder nachdem die Speicherung nicht mehr erforderlich ist, sofern nicht gesetzliche Aufbewahrungspflichten bestehen oder Verjährungsfristen beachtet werden müssen.
Rechtsgrundlage ist Art. 6 Abs. 1 b) DSGVO.
5. Rechte des Betroffenen
Sie haben als Betroffener der Datenverarbeitung folgende Rechte hinsichtlich der Sie betreffenden personenbezogenen Daten:
- Recht auf Auskunft,
- Recht auf Berichtigung oder Löschung,
- Recht auf Einschränkung der Verarbeitung,
- Recht auf Widerspruch gegen die Verarbeitung,
- Recht auf Datenübertragbarkeit.
Sie haben zudem das Recht, sich bei einer Datenschutz-Aufsichtsbehörde über die Verarbeitung Ihrer personenbezogenen Daten durch uns zu beschweren.
6. Weitergabe an Behörden
Wir behalten uns im Falle einer gesetzlichen Verpflichtung vor, Informationen über Sie offen zu legen, wenn die Herausgabe von rechtmäßig handelnden Behörden oder Strafverfolgungsorganen von uns verlangt wird.
Impressum
Kontaktdetails
RaDes GmbH
Schnackenburgallee 114
D-22525 Hamburg
E-mail: info@rades-development.com
Vertretungsberechtigter: Dr. Michael E. Herbig, Geschäftsführer
Anschrift wie oben.
Register und Registernummer: Registergericht Hamburg, HRB 152151
Umsatzsteueridentifikationsnummer: DE319530136
Publikationen
- Lunter D, Gorissen S, Herbig ME, Hukauf M, Eichner A, Reflection paper on the APV workshop on in vitro performance testing of topically applied and topically acting substances, Eur J Pharm Biopharm (220), 2026, 114971
- Surber C, Herbig ME, Reinau-Häberlin D, The Crux of vehicle designations: The essence of topical dermatologic vehicles and their use, Journal of Pharmaceutical Sciences, 2025, 104109
- Evers DH, Giebel J, Nienau F, Carle S, Gorissen S, Buske J, Herbig ME, Garidel P, Hagelskamp E, Unravelling the polysorbate 20 composition: A fusion of UPLC-MS analysis and stochastic modelling, Eur J Pharm Biopharm (216), 114854, 2025
- Schoenfelder H, Reuter M, Evers D, Herbig ME, Lunter DJ, Ceramide Profiling of Porcine Skin and Systematic Investigation of the Impact of Sorbitan Esters (SEs) on the Barrier Function of the Skin. Molecular Pharmaceutics, 22 (4), 2019-2028, 2025
- Hsiao W-K, Herbig ME, Newsam JM, Gottwald U, May E, Winckle G, Birngruber T. Opportunities of topical drug products in a changing dermatological landscape. European Journal of Pharmaceutical Sciences, Volume 203, 106913, 2024
- Carle S, Evers DH, Hagelskamp E, Garidel P, Buske J. All-in-one stability indicating polysorbate 20 degradation root-cause analytics via UPLC-QDa, Journal of Chromatography B, Volume 1232, 2024,123955
- Herbig ME, Evers DH, Gorissen S, Köllmer M. Rational Design of Topical Semi-Solid Dosage Forms-How Far Are We? Pharmaceutics 15, 1822, 2023
- Sailer MM, Köllmer M, Masson B, Fais F, Hohenfeld IP, Herbig ME, Koitschev AK & Becker S. Nasal residence time and rheological properties of a new bentonite-based thixotropic gel emulsion nasal spray – AM-301, Drug Development and Industrial Pharmacy, 2023
- Herbig, ME. Topical Drug Delivery and the Role of Excipients, Chimica Oggi – Chemistry Today, 40 (6), 34-37, 2022
- Fronk V, Schäffler M, Bonyadi H, Herbig ME, Köllmer M, Die Produktion pharmazeutischer Emulsionen optimieren. Nachrichten aus der Chemie, 70, 49-51, 2022
- Kapoor K, Gräfe N, Herbig ME, Topical film-forming solid solutions for enhanced dermal delivery of the retinoid tazarotene, Journal of Pharmaceutical Sciences, (111), 2779-2787, 2022
- Evers DH, Carle S, Lakatos D, Hämmerling F, Garidel P, Buske J. Hydrolytic polysorbate 20 degradation – Sensitive detection of free fatty acids in biopharmaceuticals via UPLC-QDa analytics with isolator column, Journal of Chromatography B, Volume 1174, 2021, 122717.
- Evers DH, Schultz-Fademrecht T, Garidel P, Buske J. Development and validation of a selective marker-based quantification of polysorbate 20 in biopharmaceutical formulations using UPLC QDa detection, Journal of Chromatography B, Volume 1157, 2020, 122287.
- Puschmann J, Evers DH, Müller-Goymann CC, Herbig ME. Development of a Design of Experiments optimized method for quantification of polysorbate 80 based on oleic acid using UHPLC-MS. J. Chrom. A, (1599): 136-143, 2019.
- Puschmann J, Herbig ME, Müller-Goymann CC. Influence of emulsifier concentration on partition behavior and chemical stability of betamethasone dipropionate in emulsion gels. Int. J. Pharm, (562): 105-112, 2019.
- Köllmer M, Mossahebi P, Sacharow E, Gorissen S, Gräfe N, Evers DH, Herbig ME. Investigation of the Compatibility of the Skin PAMPA Model with Topical Formulation and Acceptor Media Additives Using Different Assay Setups. AAPS PharmSciTech, 20(89), 2019.
- Puschmann J, Herbig ME, Müller-Goymann CC. Correlation of antimicrobial effects of phenoxyethanol with its free concentration in the water phase of o/w-emulsion gels. Eur J Pharm Biopharm, (131): 152–161, 2018.
- Blenner SR, Köllmer M, Rouse AJ, Daneshvar N, Williams C, Andrews LB. Privacy Policies of Android Diabetes Apps and Sharing of Health Information. JAMA, 315(10): 1051-52, 2016.
- Herbig ME, Houdek P, Gorissen S, Brandner J et al. A custom tailored model to investigate skin penetration in porcine skin and its comparison with human skin. Eur J Pharm Biopharm, (95): 99-109, 2015.
- Köllmer M, Appel A, Somo S, Brey E. Long-Term Function of Alginate Encapsulated Islets. Tissue Engineering Part B: Reviews, 22(1), 2015. DOI: 10.1089/ten.TEB.2015.0140.
- Sharma V, Köllmer M, Szymusiak M, Nitsche LC, Gemeinhart RA, Liu Y. Toroidal-spiral particles for codelivery of anti-VEGFR-2 antibody and irinotecan: a potential implant to hinder recurrence of glioblastoma multiforme. Biomacromolecules, 15(3): 756-62, 2014.
- Zhang Y, Köllmer M, Buhrman JS, Tang MY, Gemeinhart RA. Arginine-rich, cell penetrating peptide-anti-microRNA complexes decrease glioblastoma migration potential. Peptides, 58: 83-90, 2014.
- Herbig ME, Evers DH. Correlation of hydrotropic solubilization by urea with log D of drug molecules and utilization of this effect for topical formulations. Eur J Pharm Biopharm, 85(1): 158-160, 2013.
- Köllmer M, Buhrman JS, Zhang Y, Gemeinhart RA. Markers Are Shared Between Adipogenic and Osteogenic Differentiated Mesenchymal Stem Cells. Journal of Developmental Biology and Tissue Engineering, 5(2): 18-25, 2013.
- Köllmer M, Popescu C, Manda P, Zhou L, Gemeinhart RA. Stability of Benzocaine Formulated in Commercial Oral Disintegrating Tablet Platforms. AAPS PharmSciTech, 14(4):1333-40, 2013.
- Köllmer M, Keskar V, Hauk TG, Collins JM, Russell B, Gemeinhart RA. Stem Cell-Derived Extracellular Matrix Enables Survival and Multilineage Differentiation within Superporous Hydrogels. Biomacromolecules, 13(4): 963-973, 2012.
- Buhrman JS, Rayahin JE, Köllmer M, Gemeinhart RA. In-house preparation of hydrogels for batch affinity purification of glutathione S-transferase tagged recombinant proteins. BMC Biotechnology, 12(1): 63, 2012.
- Herbig ME, Weller K, Merkle HP. Reviewing biophysical and cell biological methodologies in cell penetrating peptide research. Critical Rev. in Therapeutic Drug Carrier Systems, 24(3): 203-255, 2007.
- Herbig ME, Assi F, Textor M, and Merkle HP. The cell penetrating peptides pVEC and W2-pVEC induce transformation of gel phase domains in phospholipid bilayers without affecting their integrity. Biochemistry, 45(11): 3598-3609, 2006.
- Herbig ME, Weller K, Krauss U, Beck-Sickinger AG, Merkle HP, and Zerbe O. Membrane surface-associated helices promote lipid interactions and cellular uptake of human calcitonin-derived cell penetrating peptides. Biophysical Journal, 89(6): 4056-4066, 2005.
- Herbig ME, Fromm U, Leuenberger J, Krauss U, Beck-Sickinger AG, and Merkle HP. Bilayer interaction and localization of cell penetrating peptides with model membranes. Biochimica et Biophysica Acta-Biomembranes, 1712(2): 197-211, 2005.
Unsere Werte
Es ist für uns Antrieb und Motivation, einen Beitrag zur Entwicklung von Medikamenten zu leisten, die helfen, die Lebensqualität von Patienten zu erhöhen und Leiden zu mildern.
Aus vielen Jahren Erfahrung in der pharmazeutischen Entwicklung dermatologischer Arzneimittel wissen wir, dass gute Medikamente einen wichtigen Beitrag zur Lebensqualität von Patienten leisten. Dass wir als Entwickler hier einen Beitrag leisten können, ist ein wichtiger Aspekt unserer täglichen Motivation.
Dermatologische Erkrankungen sind zwar selten lebensbedrohlich (und selten ansteckend), werden aber stark wahrgenommen – sowohl direkt über die Haut als größtes Sinnesorgan des Menschen, als auch indirekt über ihre häufig für andere sichtbare Manifestation, die belastend wirken kann.
Dermatika sind dem Anwender im wörtlichen Sinne „näher“ als die meisten anderen Arzneimittel. Gut entwickelte Produkte können – auch über die in Studien erfasste klinische Wirksamkeit hinaus – wesentlich zum Therapie-Erfolg und zu einer gesteigerten Lebensqualität beitragen. Dazu kann eine bequeme und sichere Handhabung, gute Verträglichkeit unter Berücksichtigung des spezifischen Hautzustandes und eine angenehme Kosmetik beisteuern. Allen voran aber trägt zum Fortschritt bei, anspruchsvolle Formulierungsherausforderungen überhaupt zu lösen und damit vielversprechende Wirkstoffe als Medikament auf dem Markt zu bringen und den Patienten zur Verfügung zu stellen. Dafür engagieren wir uns mit unserem Wissen, unserer Kreativität und Ausdauer.
Wir glauben, dass der Wille zur permanenten Weiterentwicklung, sowie die Beharrlichkeit und Entschlossenheit, auch schwierige Probleme erfolgreich zu lösen, wichtige Erfolgsfaktoren sind und leben diese Einstellung.
Halbfeste Arzneiformen sind vielfältig, häufig komplex, und machen einen eher kleinen Anteil an der Summe der entwickelten Arzneimittel aus. Deshalb sind viele dieser Systeme, auch die klassische Creme, allgemein noch weit weniger gut verstanden als z.B. Tabletten oder Kapseln. Damit ist es herausfordernder, sie systematisch, robust und ökonomisch zu entwickeln. Das Team der RaDes GmbH hat in jahrzehntelanger Erfahrung nicht nur viele Formulierungen entwickelt, sondern immer auch in ein besseres wissenschaftlich-technisches Verständnis der Grundlangen der Entwicklung topischer Formulierungen investiert. Dieses Verständnis erlaubt uns ein weitgehend „rationales Design“ von Formulierungen, d.h. ein systematisches, zielgerichtetes Vorgehen, durch das Irrwege und nachträgliche Änderungen minimiert werden können. Auf diesem Weg erhalten wir auch Antworten, warum etwas funktioniert oder nicht, identifizieren Stellschrauben für gezielte Modifikationen und sind in der Lage, auch schwierigste Herausforderungen im Formulierungsdesign und der Analytik zu lösen. Außerdem bildet es das Fundament, das Innovationen ermöglicht. Wir sind außerdem überzeugt, dass ein solch systematisches Verständnis von Formulierungen mittel- und langfristig ein erhebliches ökonomisches Einsparpotential bedeutet, da späteres Troubleshooting vermieden oder deutlich gezielter durchgeführt werden kann.
Aus unserer Erfahrung glauben wir fest daran, dass sich lebendige wissenschaftliche Neugier und beharrliches Bemühen um bessere Lösungen auszahlen. In Kollaborationen mit Universitäten, Lieferanten und Partnerunternehmen und unter Einsatz von moderner Software arbeiten wir weiter daran, dieses Verständnis noch zu vertiefen, um immer bessere Lösungen zu liefern.
Wir wollen durch verantwortungsvolles, professionelles und faires Handeln einen positiven gesellschaftlichen Beitrag leisten.
Wir haben uns entschlossen, ein Unternehmen zu gründen, weil wir bereit sind, Verantwortung zu übernehmen und weil wir es schätzen, im Einklang mit unseren Überzeugungen gestalten zu können.
Inspiriert durch das Leitbild des „ehrbaren hanseatischen Kaufmanns“, sind uns Fairness, Verlässlichkeit und langfristige Orientierung genauso wichtig wie das Bestreben, nachhaltige win-win-Situationen mit unseren Geschäftspartnern zu generieren und gesellschaftliche Verantwortung zu tragen.
Wir wollen Arbeitsplätze schaffen und uns bereitet es Freude, Mitarbeiter weiterzuentwickeln und ihnen die Möglichkeit zu geben, basierend auf ihren individuellen Stärken zu wachsen. Ebenso engagieren wir uns, zum wissenschaftlichen Fortschritt auf unserem Arbeitsgebiet durch Forschung und aktiver Teilnahme am Diskurs beizutragen.
Sascha Gorissen
Sascha Gorissen leitet den Laborbetrieb und das Projektmanagement der RaDes GmbH. Zudem verantwortet er den Bereich der bei RaDes implementierten in vitro/ex vivo Modelle zur Freisetzung und perkutanen Absorption. Er absolvierte ein Ingenieurstudium an der Fachhochschule in Gießen mit Studienrichtung Biotechnologie und begann seine berufliche Laufbahn als wissenschaftlicher Mitarbeiter in der präklinischen Entwicklung der Firma Schwarz Pharma AG in Monheim. Schwerpunkt seiner Arbeit in den Abteilungen Molekularbiologie und ADME lag in der Etablierung und Durchführung von molekularbiologischen und zellbiologischen Methoden. Weiterhin war er für die Entwicklung, Validierung und Durchführung bioanalytischer Methoden im GLP-Bereich verantwortlich.
Anschließend war er als wissenschaftlicher Mitarbeiter in der Analytik bei der AMDS GmbH für die Erweiterung des analytischen Methodenspektrums und Organisation des Labors verantwortlich. Zudem etablierte er eine präparative HPLC-Methode zur Aufreinigung chiraler Substanzen. 2009 erfolgte der Wechsel zu Almirall Hermal. Dort war er in der Gruppe Analytik und Qualitätskontrolle zunächst verantwortlich für die Entwicklung und Validierung analytischer Methoden für halbfeste Arzneimittel unter GMP, Implementierung neuer analytischer Technologien wie Massenspektrometrie, Ermittlung von Strukturinformationen unbekannter Abbauprodukte und Qualifizierung computergestützter Systeme. Weiterhin übernahm er die CMC-Leitung verschiedener internationaler Entwicklungsprojekte von Machbarkeit bis zur klinischen Phase III.
Von 2016 bis zur Gründung der RaDes GmbH war er als Gruppenleiter der „Analytik und Qualitätskontrolle Pharmazeutische Entwicklung“ am Standort Reinbek tätig.
Dr. Melanie Köllmer
Dr. Melanie Köllmer leitet die Formulierungsentwicklung der RaDes GmbH. Sie verfügt über zehn Jahre Erfahrung in der pharmazeutischen und biomedizinischen Forschung. Ihre Expertise liegt in der Umsetzung von Entwicklungsprojekten angefangen bei der Formulierungsentwicklung im Rahmen von Feasibility-Studien bis hin zur Implementierung in der klinischen Phase und Prozessentwicklung von halbfesten Arzneiformen.
Sie studierte Pharmazie an der Philipps-Universität Marburg und promovierte auf dem Gebiet Drug Delivery und Tissue Engineering an der University of Illinois at Chicago, USA, im Labor von Prof. Dr. Richard A. Gemeinhart, gefolgt von einem Postdoc-Programm am Illinois Institute of Technology (IIT).im Labor von Prof. Dr. Eric Brey.
Im Anschluss daran war sie als Formulation Scientist bei Almirall Hermal tätig. In enger Zusammenarbeit mit der analytischen Entwicklung sowie Drug Discovery, Intellectual Property und Regulatory Affairs, beschäftigte sie sich umfassend mit dem Design von halbfesten Formulierungen, sowie mit der Evaluierung von neuen topischen Hilfsstoffen und Technologieplattformen. Insbesondere leistete sie entscheidende Beiträge zur erfolgreichen Entwicklung einer hydrophilen Tacrolimus-Creme (Patent WO2019233722).
Sie beschäftigt sich mit rationalem Design, kosmetischer Optimierung und Charakterisierung von halbfesten Formulierungen für „small molecules“ und Probiotika. Ein besonderer Schwerpunkt ist die Nutzung moderner rheologischer Verfahren zur Optimierung von Stabilität, Herstellprozessen und Anwenderfreundlichkeit.
Melanie Köllmer ist Autorin von bisher neun Publikationen im Bereich Drug Delivery und in vitro Performance Tests in international anerkannten Peer-Review-Fachzeitschriften und hält regelmäßig Vorträge im Bereich Formulierungsentwicklung und Rheologie.
















 PETRA LOHMANN
PETRA LOHMANN SASCHA GORISSEN
SASCHA GORISSEN MELANIE KÖLLMER
MELANIE KÖLLMER